Аккумуляторы
· Пример 1. Четыре гальванических элемента, у которых э. д. с. каждого Е0 = 1,6 в и внутреннее сопротивление r0=8 ом, соединены параллельно. Определить силу тока в цепи, если батарея замкнута на внешнее сопротивление 6 ом.
· Решение. Э. д. с. батареи E=1,6 в, внутреннее сопротивление ее ![]() =2 ом. 4
=2 ом. 4
· Следовательно, сила тока в цепи .
· ![]()
· .Пример 2. Последовательно соединены 10 гальванических элементов, каждый из которых имеет э. д. с. 1,2 в и внутреннее сопротивление 5 ом. Определить силу тока в цепи, если батарея замкнута на внешнее сопротивление 30 ом.
· Решение. Э. д. с. батареи E=10×1,2= 12 в. Внутреннее сопротивление батареи r== 10×5=50 ом. Следовательно, сила тока цепи 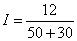 =0,15 а.
=0,15 а.
· § 29. АККУМУЛЯТОРЫ
·
· Аккумулятором называется прибор, обладающий способностью накапливать и сохранять в течение некоторого времени электрическую энергию в результате химических процессов.
· В аккумуляторе, как и в гальваническом элементе, электрический ток является следствием химических процессов. Но в отличие от аккумулятора в гальваническом элементе получающиеся химические соединения не могут быть вторично разложены и приведены в первоначальное состояние током постороннего источника. Поэтому гальванические элементы называются первичными, а аккумуляторы — вторичными или обратимыми. Повторные заряд и разряд не 1 только не вредят аккумулятору, но даже улучшают его свойства, так как в работе участвуют все более глубокие слои пластин электродов.
· В зависимости от состава электролита аккумуляторы могут быть кислотными и щелочными. Простейший кислотный аккумулятор состоит из двух свинцовых пластин (электродов), погруженных в электролит, которым служит вода с небольшим добавлением серной кислоты.
·
· Постоянный ток постороннего источника, проходя через электролит, разлагает его на составные части. Внутри электролита возникает движение положительных ионов водорода Н2 к пластине, соединенной с отрицательным зажимом источника тока, и отрицательных ионов кислорода О к пластине, соединенной с положительным зажимом источника тока. В результате электролиза окисляется свинец на положительном электроде и образуется губчатый свинец на отрицательном электроде.
·  Таким образом электрическая энергия преобразовывается в химическую и аккумулятор становится заряженным.
Таким образом электрическая энергия преобразовывается в химическую и аккумулятор становится заряженным.
· Химическая энергия может сохраняться определенное время и при надобности легко переходит в электрическую.
· Если аккумулятор отключить от источника тока и замкнуть на какой-нибудь приемник энергии, то аккумулятор сам станет источником тока подобно гальваническому элементу, у которого электродами служат пластины, отличающиеся друг от друга по химическому составу
· Электролитом в кислотных аккумуляторах, как указывалось выше, служит раствор серной кислоты определенной плотности. Плотностью раствора или его удельным весом называется число, показывающее, во сколько раз вес этого раствора больше веса воды того же объема.
· Для наполнения стационарных аккумуляторов употребляют раствор серной кислоты плотностью 1,21 при 15° С. Для переносных аккумуляторов применяют раствор серной кислоты плотностью 1,26.
· Плотность электролита определяют ареометром. Он представляет собой стеклянную трубку, запаянную с обеих концов и имеющую внутри шкалу с делениями. В нижней расширенной части ареометра находится ртуть или дробь, в результате чего трубка плавает вертикально. Ареометр опускают в сосуд с электролитом. Чем больше плотность электролита, тем выше поднимается ареометр из жидкости. Деление ареометра, расположенное на уровне раствора, показывает плотность электролита.
· При составлении раствора для аккумуляторов серную кислоту тонкой струей наливают в воду. Нельзя вливать в серную кислоту воду, так как произойдет бурное разбрызгивание кислоты, которая может причинить ожоги. Вода для электролита должна быть дистиллированной.
· Внутреннее сопротивление аккумуляторов очень мало по сравнению с внутренним сопротивлением гальванических элементов. Это дает возможность считать напряжение на зажимах аккумуляторной батареи примерно равным ее э. д. с. Однако внутреннее сопротивление не является постоянной величиной. Оно определяется составом пластин, расстоянием между ними, плотностью и температурой электролита, степенью заряженности аккумулятора. Так, сопротивление разряженного аккумулятора примерно в полтора — два раза больше, чем заряженного.
· Э. д. с. аккумулятора зависит от плотности электролита и не зависит от его размеров и номинальной емкости. При плотностях электролита d в пределах 1,1—1,35 э. д. с. аккумулятора
· ![]()
· В процессе заряда и разряда аккумулятора плотность электролита не остается постоянной, в связи с этим изменяется как его э. д. с, так и напряжение на его зажимах.
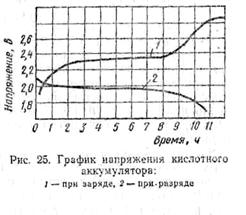
· При заряде кислотного аккумулятора напряжение его сравнительно быстро возрастает до 2,2 в (рис. 25, кривая 1), затем медленно достигает 2,3 в, после чего довольно быстро возрастает до 2,6 в и, наконец, медленно увеличивается до 2,7—2,75 в и выше не поднимается.
· По достижении напряжения 2,2 в у отрицательной пластины аккумулятора начинают выделяться пузырьки водорода, а при 2,3 в около положительной пластины появляются пузырьки кислорода.
При 2,5 в около обеих пластин происходит обильное выделение газов, а когда напряжение достигает 2,6—2,75 в аккумулятор, как говорят, начинает «кипеть». I
· При заряде аккумулятора увеличивается плотность электроли-1 та, вследствие чего напряжение на зажимах аккумулятора повышается. При напряжении 2,4—2,5 в аккумулятор полностью зарядится (заканчивается процесс восстановления активной массы). При дальнейшем процессе заряда происходит электролиз воды, при котором пластины аккумулятора покрываются пузырьками водорода и кислорода, что уменьшает активную поверхность пластин, увеличивая внутреннее сопротивление аккумулятора, вследствие чего увеличивается напряжение на его зажимах. Так как бурное выделение кислорода и водорода разрушает пластины, то в конце заряда следует уменьшить силу зарядного тока.
· При разряде кислотного аккумулятора напряжение на его зажимах быстро падает до 2—1,95 в (рис. 25, кривая 2), затем медленно понижается до 1,86—1,8 в и после этого снова быстро уменьшается до нуля.
· Понижение напряжения при разряде аккумулятора объясняется тем, что при разряде плотность его электролита уменьшается. Когда напряжение на аккумуляторе достигает значения 1,8 в (при кратковременном разряде 1,75 в), это значит, что вся запасенная в нем энергия израсходована (на обеих пластинах образуется сернокислый свинец, являющийся плохим проводником тока). При дальнейшем разряде напряжение быстро уменьшается до нуля. Если аккумулятор отключить от нагрузки, то его напряжение вновь увеличится примерно до 2 в, так как электролит проникает в глубь
· пластин в поры активной массы. Однако при включении такого аккумулятора вновь на нагрузку напряжение на его зажимах опять быстро уменьшится до нуля.
· Практически разряд доводят только до 1,8 в, так как при разряде ниже 1,8 в аккумулятор приходит в негодность — пластины его частично покрываются белым налетом крупнокристаллического сернокислого свинца, который представляет собой настолько плохой проводник, что заряд аккумулятора до номинальной емкости становится невозможным. Это явление называется сульфатацией пластин аккумулятора.
· Количество электричества, которое аккумулятор может отдать при разряде определенным током до наинизшего допустимого напряжения, называется его емкостью. Она равна произведению разрядного тока в амперах на продолжительность времени разряда в часах и выражается в ампер-часах.
· Емкость аккумулятора зависит от количества активной массы, величины тока и температуры. Под номинальной емкостью понимают то количество электричества, которое отдает полностью заряженный аккумулятор при 10-часовом режиме разряда и температуре 25° С. Таким образом, аккумулятор отдает номинальную емкость, разряжаясь в течение 10 ч током, численно равным 0,1 величины его номинальной емкости. При увеличении разрядного тока емкость аккумулятора уменьшается, так как поверхность пластин покрывается сернокислым свинцом и затрудняет доступ электролита к внутренним слоям активной массы. При понижении температуры увеличивается вязкость электролита, что также затрудняет его доступ к внутренним слоям активной массы и уменьшает емкость аккумулятора.


