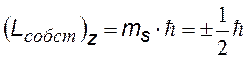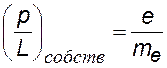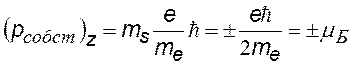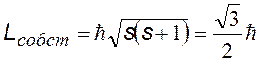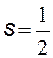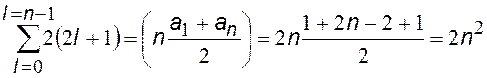Магнитное собственное квантовое число
![]()
![]()
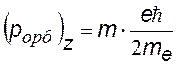
![]()
|
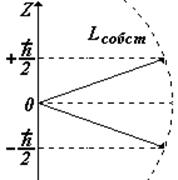
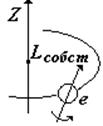
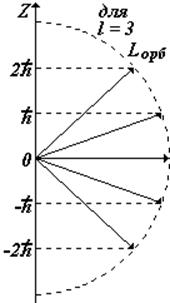
4) Входит в выражение для проекций собственного механического Lсобст и магнитного рсобст моментов на направление Z внешнего поля (например, магнитного). Показывает, что ориентация Lсобст (спина –см. дальше) может иметь только два значения. |
||
|
|
|
|
|
|
отношение собственных магнитного и механического моментов |
|
Спин (от англ. spin — веретено). Спином называется собственный механический момент (момент импульса) электрона |
|
|
|
Спин — собственный механический момент (момент импульса) электрона – имеет только одно значение. Спин связан со спиновым квантовым числом s, имеющим также только одно значение ½. |
|
|
спиновое квантовое число |
|
В квантовой механике различают частицы с «целым» спином (бозоны) и «полуцелым» спином (фермионы, например, электрон, см. дальше).Это условная терминология. Из формулы для спина видно, что он не может быть целым числом. В этих словах подразумевается, что проекция спина либо кратна |
|
Таким образом, из квантовой механики следует, что энергия электрона, его орбитальные моменты, проекции орбитальных моментов на внешнее поле — квантуются. Они не могут иметь любые значения, а только те, которые определяются приведенными выше соотношениями. Собственный момент электрона имеет только одно значение, а его проекция на внешнее поле – два значения ± ![]() / 2. Часто условно говорят «спин вверх», «спин вниз».
/ 2. Часто условно говорят «спин вверх», «спин вниз».
 Чтобы представить сложность поведения электрона даже в простейшем атоме Н, на рисунке представлена плотность вероятности для электрона в состоянии с n = 4, l = 2, m = ± 1. Светлые пятна — это области, в которых наиболее вероятно пребывание электрона. Это только плоский срез, в действительности вероятность имеет объемное распределение.
Чтобы представить сложность поведения электрона даже в простейшем атоме Н, на рисунке представлена плотность вероятности для электрона в состоянии с n = 4, l = 2, m = ± 1. Светлые пятна — это области, в которых наиболее вероятно пребывание электрона. Это только плоский срез, в действительности вероятность имеет объемное распределение.
Принцип Паули. Периодическая система элементов.
В 1925 г Паули, исследуя спектры многоэлектронных атомов, открыл фундаментальный закон, которому подчиняются электронные конфигурации атомов, имеющих более одного электрона. Принцип Паули: «Никакие два электрона в атоме не могут находиться в одном и том же квантовом состоянии, каждый электрон должен иметь свой набор квантовых чисел
n, l, m, ms». Принципу Паули подчиняются не все микрочастицы, а только те, которые имеют полуцелый спин – электрон, протон, нейтрон, нейтрино. Частицы с полуцелым спином называют фермионами (см. дальше). Принцип Паули объясняет, почему электроны в многоэлектронных атомах образуют энергетические оболочки и подоболочки.
Распределение электронов в атомах определяется:
1) принципом Паули и
2) принципом наименьшей энергии [xvii]
Найдем количество электронов, имеющих заданные квантовые числа.
|
заданные квантовые числа |
n, l, m, ms |
n, l, m |
n, l |
n |
|
количество электронов |
1 |
2 |
2(2l + 1) |
2 n2 |
Магнитное собственное квантовое число ms может принимать два значения, поэтому принцип Паули формулируют еще и так: в одном энергетическом состоянии могут находиться два электрона, но с разнонаправленными спинами. Общее число орбитальных квантовых чисел m равно (2l + 1). Количество электронов с одинаковыми n можно найти как алгебраическую сумму
|
|
Удобно представить заполнение электронами оболочек и подоболочек
атомов в виде таблицы.
|
n |
обо-лоч- ки |
подоболочки l = |
макс. число эл-нов в оболочке |
||||
|
0 |
1 |
2 |
3 |
4 |
|||
|
s |
p |
d |
f |
g |
|||
|
1 |
K |
2 |
— |
— |
— |
— |
2 |
|
2 |
L |
2 |
6 |
— |
— |
— |
8 |
|
3 |
M |
2 |
6 |
10 |
— |
— |
18 |
|
4 |
N |
2 |
6 |
10 |
14 |
— |
32 |
|
5 |
O |
2 |
6 |
10 |
14 |
18 |
50 |
Подобное распределение является идеализированным. Оно было бы таким, если бы каждый электрон в атоме взаимодействовал только с ядром атома. В действительности данный электрон испытывает действие остальных электронов атома. Часто энергетически выгодным оказывается состояние, когда нижняя оболочка заполнена неполностью, а начинает заполняться следующая. Нарушения в заполнении электронных оболочек атомов наблюдаются у № 19 – калий и более тяжелых элементов.
Электронную конфигурацию атомов принято выражать формулой:
|
|
Здесь 1, 2, 3,… — главные квантовые числа,
s, p, d,… — буквенные обозначения орбитальных квантовых чисел l, верхние числа – количество электронов с данными n и l . Сумма верхних чисел дает общее количество электронов в данном атоме.
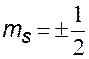 ms — магнитное собственное квантовое число;
ms — магнитное собственное квантовое число;